Тема 2.
Химический состав клетки.
Часть 1
Химический состав клетки.
Часть 1
!Из 112 химических элементов периодической системы
Д. И. Менделеева в клетках живых организмов обнаружено примерно 25!
Д. И. Менделеева в клетках живых организмов обнаружено примерно 25!
Ультрамикроэлементы
(менее ~0,001%)
(менее ~0,001%)
Макроэлементы
(~99%)
(~99%)
Микроэлементы
(~1%)
(~1%)
По количественному содержанию в клетке все химические элементы делят на 3 группы:
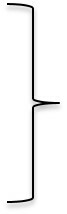
!Клетки состоят из тех же химических элементов, которые образуют неживую природу!
Макроэлементы
содержатся в десятых или сотых долях процента
кальций, фосфор,
хлор, калий, сера,
натрий, магний,
железо
хлор, калий, сера,
натрий, магний,
железо
Азот – 3%
Макроэлементы составляют основную массу вещества клетки на их долю приходится
около 99%, из них 98 % приходится на четыре химических элемента:
около 99%, из них 98 % приходится на четыре химических элемента:
Это органогенные элементы (органогены) – они входят в состав белков, нуклеиновых кислот, липидов, углеводов, воды
Углерод – 18%
Водород – 10%
Кислород – 65%
И еще 1% приходится на долю 8 элементов:
Биологическая роль некоторых макроэлементов
Магний входит в состав хлорофилла у растений; обеспечивает сердечные сокращения
Железо входит в состав гемоглобина крови, транспортирует кислород
Кальций входит в состав костей, зубов; обеспечивает свертываемость крови, сокращения мышц, работу рецепторов
Фосфор входит в состав костей, зубов, мембран
Хлор поддерживает водно-солевой баланс, торможение нервных импульсов, входит в состав соляной кислоты желудка

Калий, натрий обеспечивают электрический заряд на мембранах нервных волокон, поддерживают водно-солевой баланс

Сера входит в состав некоторых белков, больше всего в белке кератине (рога, копыта, волосы, ногти и т.п.)
Микроэлементы
Микроэлементы – преимущественно ионы металлов (кобальта, меди, цинка и др.) и галогенов (йода, брома и др.). Они содержатся в количествах от 0,001% до 0,000001%.
Входят в состав гормонов, ферментов, витаминов.
Примеры:
Цинк – необходимый элемент для работы ферментов (ДНК- и РНК- полимераз) и гормонов (инсулин).
Йод – входит в состав тироксина – гормона щитовидной железы, содержится в морских водорослях.
Медь – необходимый элемент для работы ферментов.
Фтор – входит в состав эмали зубов.
Входят в состав гормонов, ферментов, витаминов.
Примеры:
Цинк – необходимый элемент для работы ферментов (ДНК- и РНК- полимераз) и гормонов (инсулин).
Йод – входит в состав тироксина – гормона щитовидной железы, содержится в морских водорослях.
Медь – необходимый элемент для работы ферментов.
Фтор – входит в состав эмали зубов.
Ультрамикроэлементы
Ультрамикроэлементы – концентрация ниже 0,000001 %. К ним относят золото, уран, ртуть, селен и др.
Физиологическая роль большинства этих элементов в живых организмах не установлена
Физиологическая роль большинства этих элементов в живых организмах не установлена
Неорганические
Химические элементы в животной клетке
Газы (0,1-0,5%)
Высоко-молекулярные органические соединения
Минеральные соли (1-1,5%)
Органические
Вода (70-80%)
Белки (10-20%)
Липиды (1-5%)
Углеводы (1-1,5%)
Нуклеиновые кислоты (1-2%)
Низкомолекулярные органические соединения (АТФ, витамины, переносчики водорода, пигменты и др.)
Неорганические вещества
Вода
•Содержание воды в организмах составляет 60-90%.
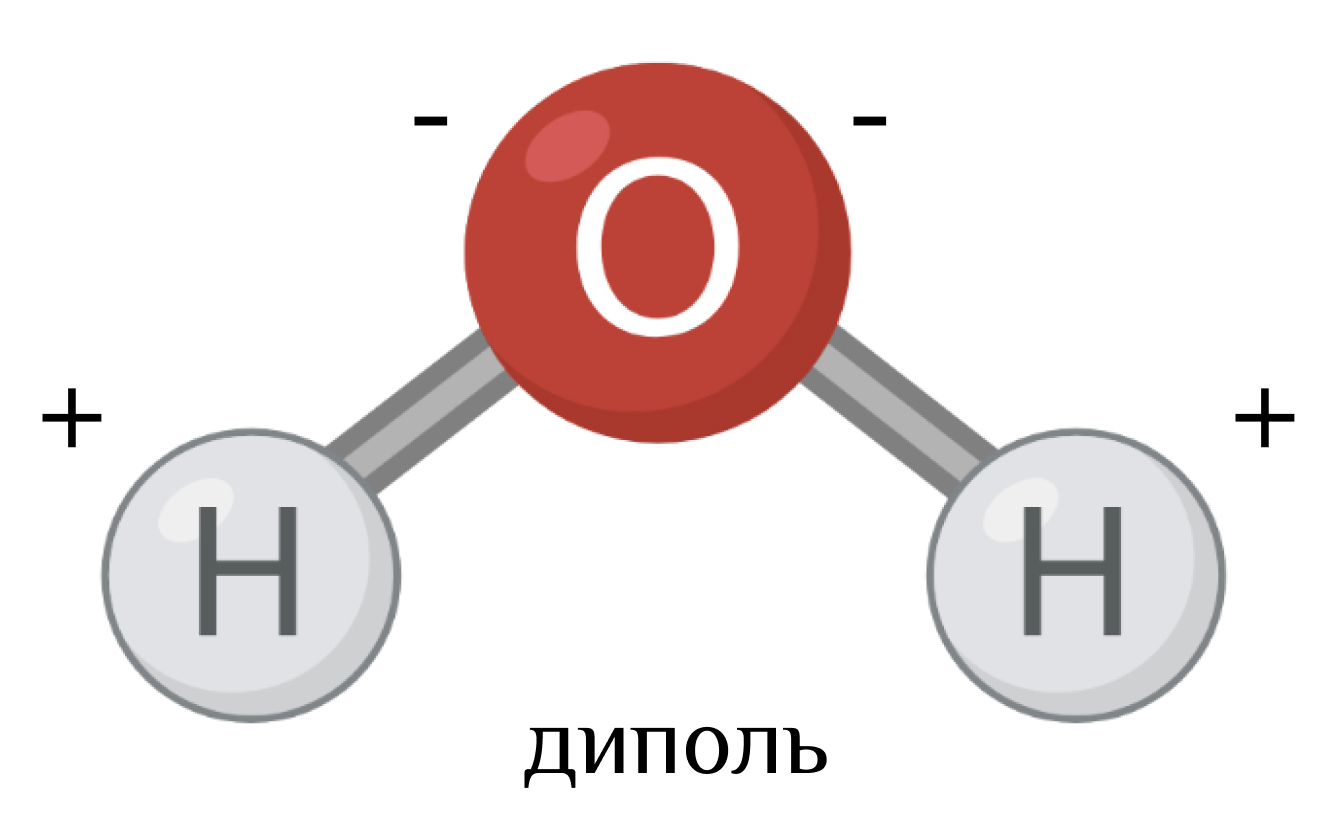
•Обладает дипольностью – атомы водорода имеет частично положительный заряд, а атом кислорода – частично отрицательный.
•95% всей воды используется как полярный растворитель и как среда для клетки.
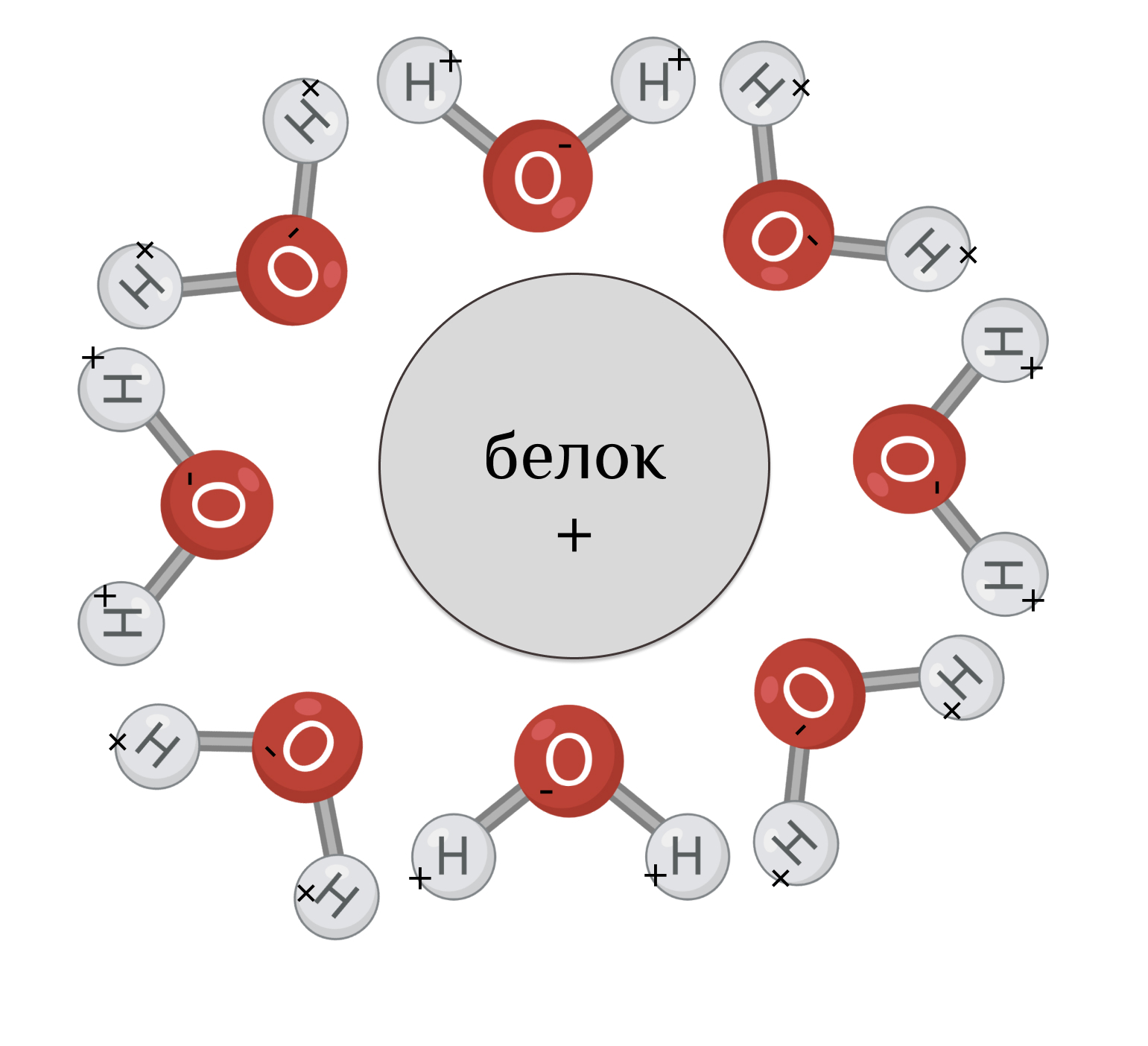
•4-5% воды связано с белками. В результате образуется водная оболочка вокруг белков, которая препятствует склеиванию их друг с другом.
•Обладает дипольностью – атомы водорода имеет частично положительный заряд, а атом кислорода – частично отрицательный.
•95% всей воды используется как полярный растворитель и как среда для клетки.
•4-5% воды связано с белками. В результате образуется водная оболочка вокруг белков, которая препятствует склеиванию их друг с другом.
Роль воды в клетке определяется ее свойствами:
- малые размеры молекул воды;
- полярность молекул;
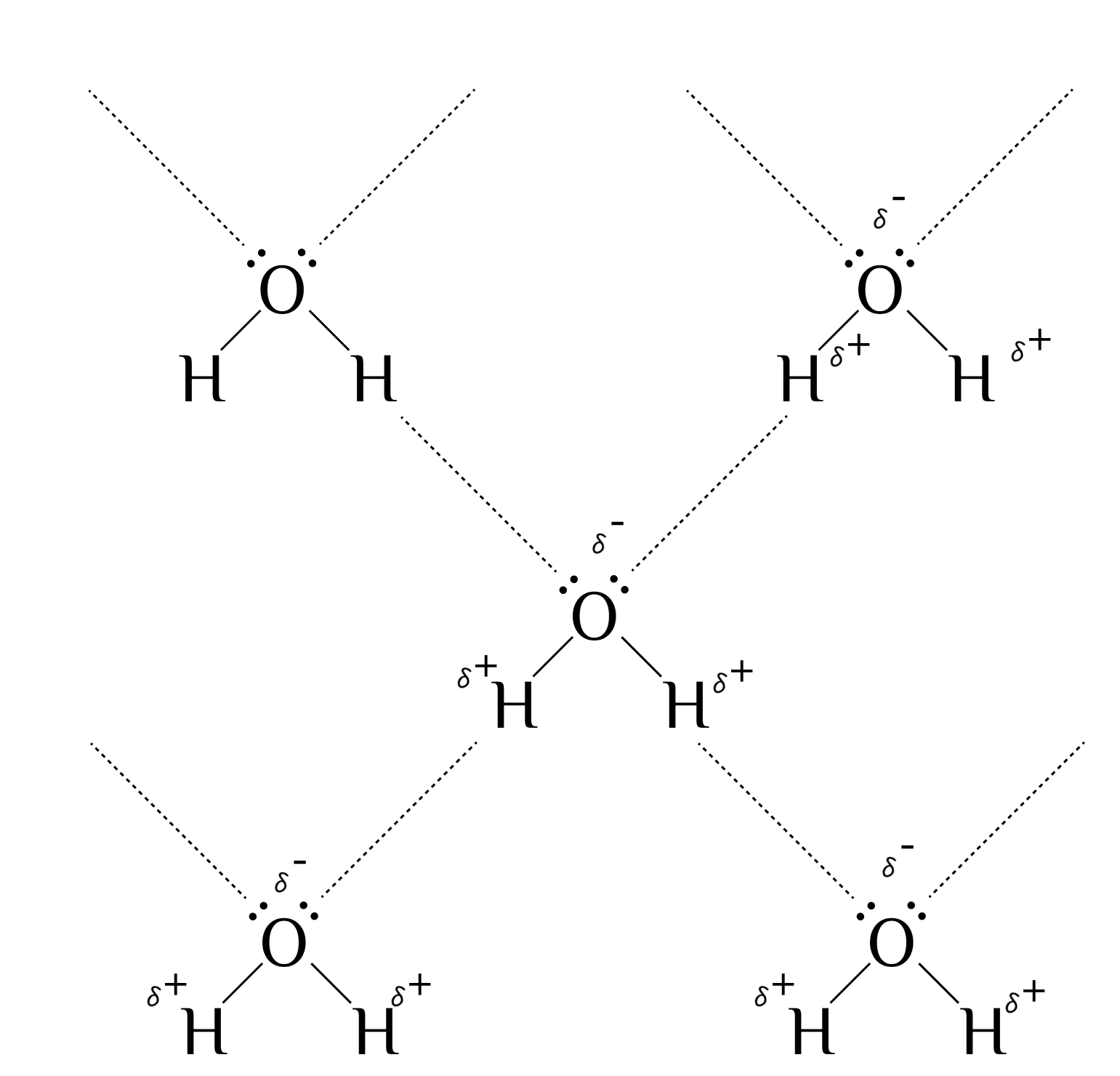
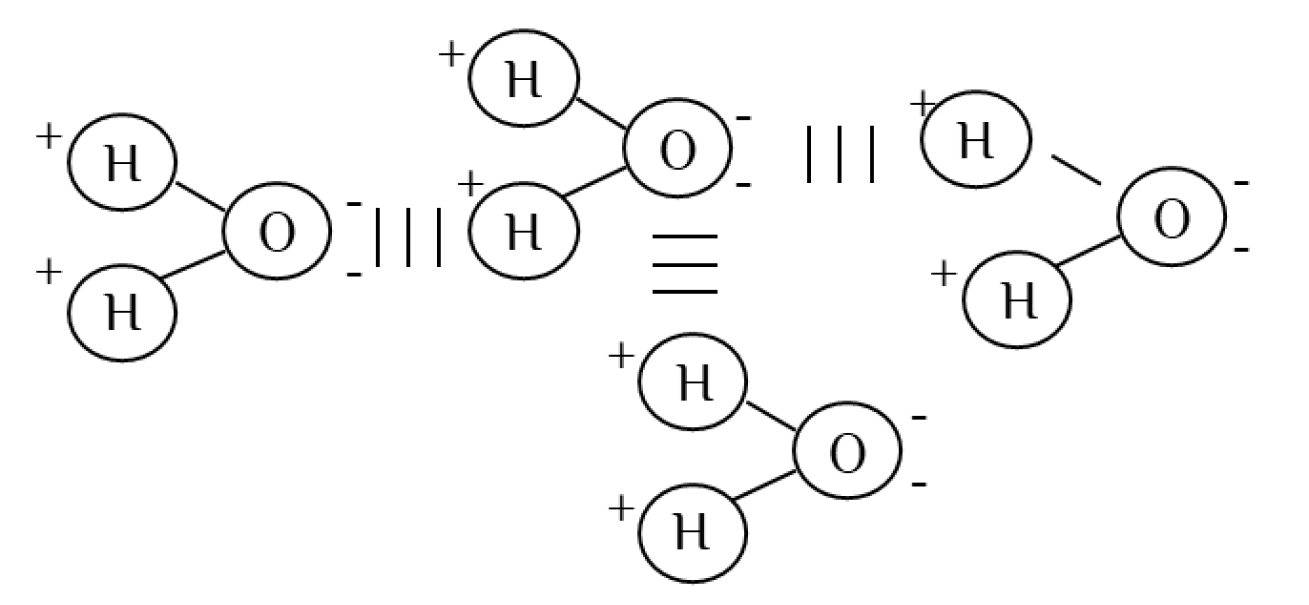
- способность соединяться друг с другом водородными связями;
- высокая удельная теплоемкость — поглощает большое количество тепловой энергии при незначительном повышении собственной температуры;
- высокая удельная теплота испарения;
- высокая теплопроводность.
Водородные связи непрочные, но их очень много!
Обычно на схемах обозначаются пунктирными линиями.
Обычно на схемах обозначаются пунктирными линиями.
Образование водородной связи
Биологическая роль воды в клетке
Универсальный растворитель
для полярных веществ: солей, сахаров, кислот и др. Вещества, растворимые в воде, называются гидрофильными;



Теплорегуляция
сохраняет тепло;

испаряясь с поверхностей, охлаждает их.
с неполярными веществами (гидрофобными) вода не образует Н-связи, а, следовательно, не растворяет их и не смешивается с ними.
Транспортная функция

транспорт веществ.



участвует в реакциях гидролиза (расщепление белков и углеводов происходит в результате их взаимодействия с водой);
определяет среду протекания химических реакций;
участвует в ОВР (например, процесс фотосинтеза).
Структурная функция
Метаболическая функция
цитоплазма клеток содержит 60-95% воды ;
обуславливает осмос и тургорное давление в клетках;
уменьшает трение.



Минеральные соли (1-1,5%)
- Катионы (NH4+, Ca2+, Na+, Fe2+ и др.)
- Анионы (Cl-, HCO3-, H2PO4-, HPO42- и др.)
Биологическая роль
• поддержание кислотно-щелочного равновесия;
• участие в создании заряда на мембране клетки;
• входят в состав ферментов;
• создание осмотического давления в клетке.
• участие в создании заряда на мембране клетки;
• входят в состав ферментов;
• создание осмотического давления в клетке.
Газы (0,1-0,5%)
- Кислород О2 — необходим для дыхания;
- Углекислый газ СО2 — необходим для фотосинтеза
- Азот N2 — необходим для жизни бактерий (хемосинтез)
- Метан CH4 — необходим для жизни бактерий (хемосинтез)
- Аммиак NH3 — необходим для жизни бактерий (хемосинтез)
Органические вещества
Низкомолекулярные органические соединения (АТФ, витамины, переносчики водорода, пигменты и др.)
Белки
Углеводы
Нуклеиновые кислоты
Липиды





Полимеры (от "поли" – много) – это вещество с высокой молекулярной массой, молекула которого состоит из большого количества повторяющихся единиц, – мономеров (от «моно» – один).
Биополимеры – полимеры, входящие в состав клеток живых организмов.
Биополимеры – полимеры, входящие в состав клеток живых организмов.
мономеры
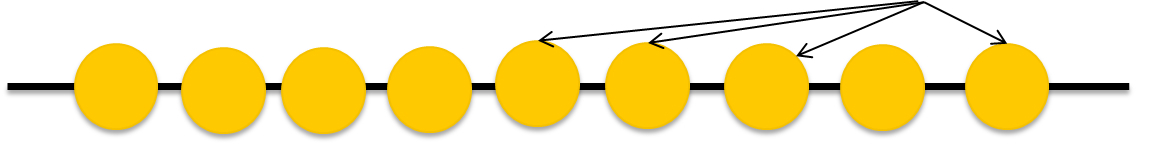
Основные биополимеры клетки
Биополимеры
Мономеры
Полисахариды
(целлюлоза, гликоген, крахмал)
(целлюлоза, гликоген, крахмал)
Нуклеиновые кислоты
Белки
Моносахариды (глюкоза)
Аминокислоты
Нуклеотиды
Белки
карбоксильная группа (кислотные свойства)
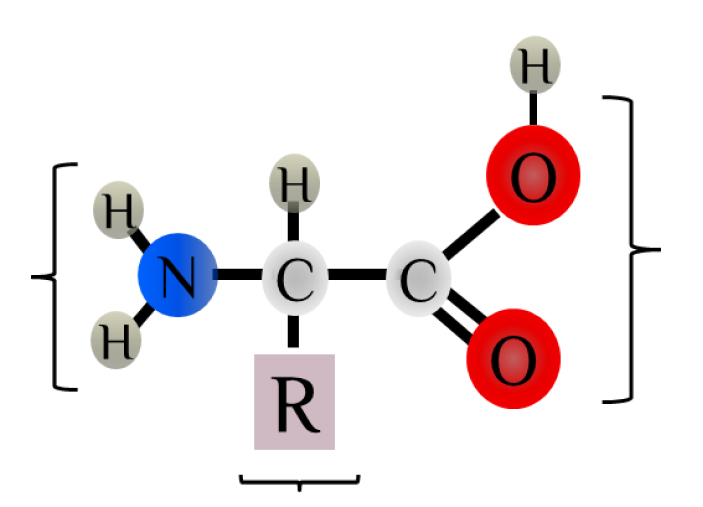
- аминокислоты отличаются одна от другой только радикалами.
радикал (20 типов)
аминогруппа (основные свойства)
Структура аминокислоты
Белки – это биополимеры, мономерами которых являются аминокислоты.
- они состоят из углерода, водорода, кислорода, азота и серы;
- в составе белков обнаружено 20 аминокислот;
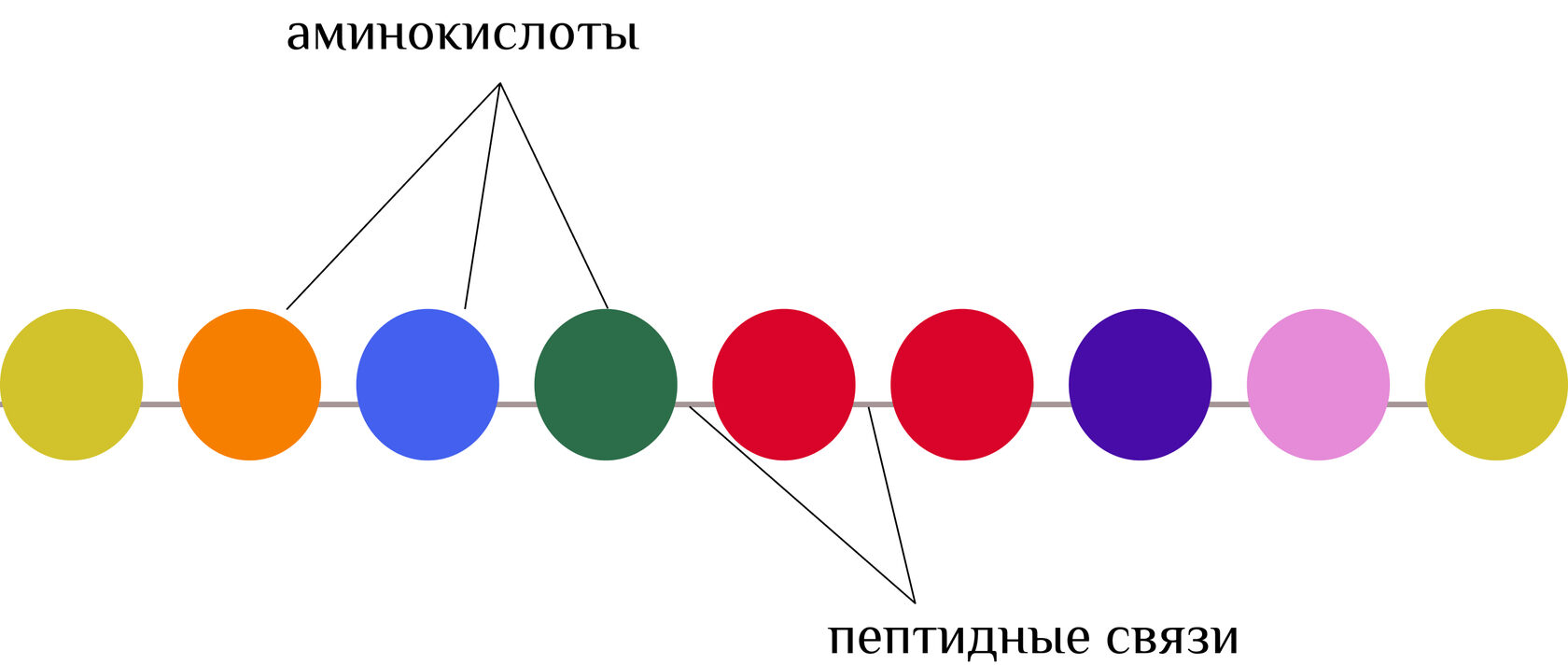
Аминокислоты
В белках аминокислоты соединены между собой пептидными связями (-NH-CO-) в полипептидные цепи.
Пептидные связи образуются при взаимодействии карбоксильной группы одной аминокислоты с аминогруппой другой.
Пептидные связи образуются при взаимодействии карбоксильной группы одной аминокислоты с аминогруппой другой.
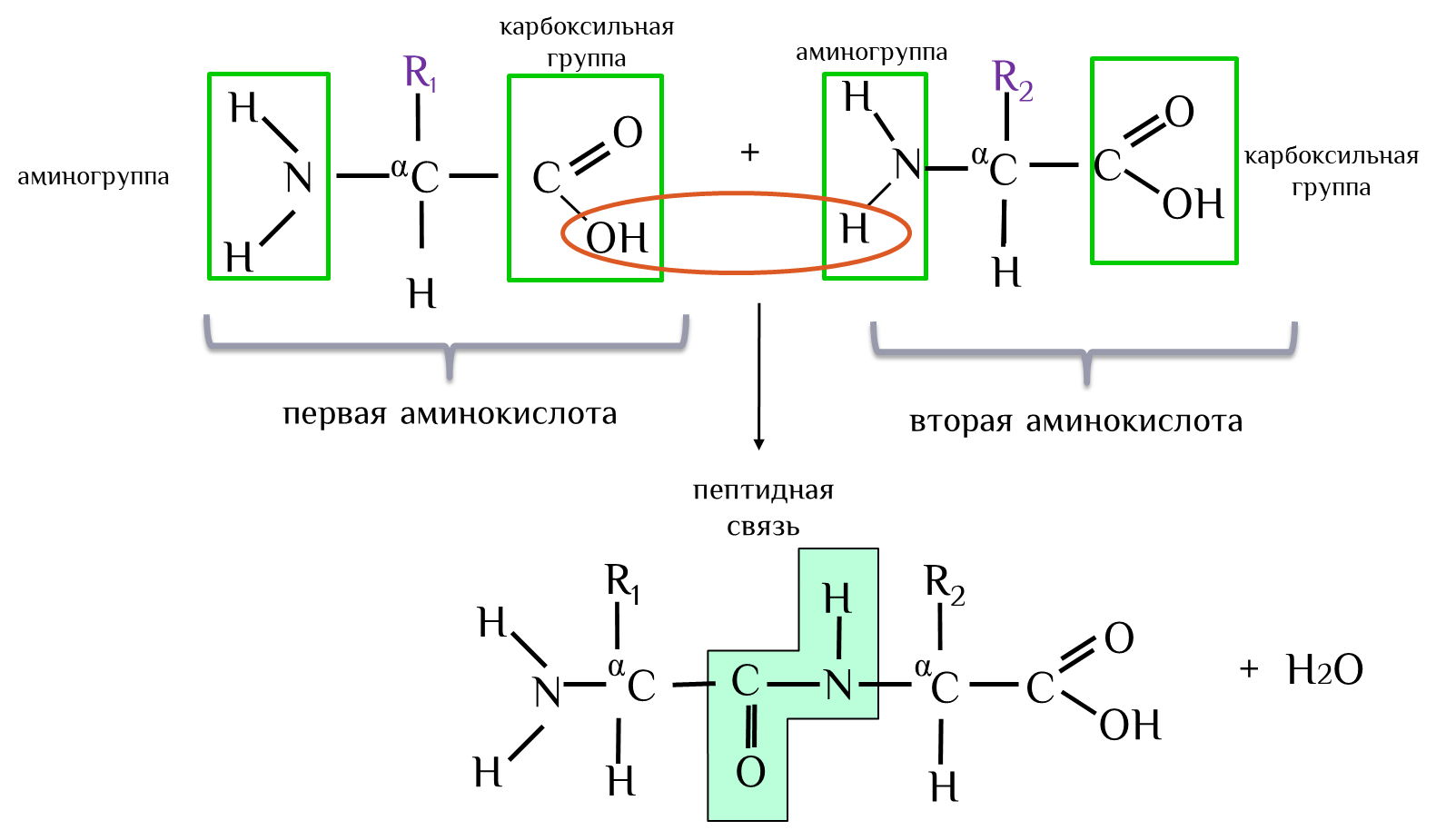
По способности человека синтезировать аминокислоты делятся на:
незаменимые аминокислоты – они не синтезируются в организме человека. Необходимо их поступление
в организм с пищей
в организм с пищей
заменимые аминокислоты – они синтезируются в организме человека в достаточном количестве
-гистидин
-изолейцин
-лейцин
-лизин
-метионин
-фенилаланин
-треонин
-триптофан
-валин
-изолейцин
-лейцин
-лизин
-метионин
-фенилаланин
-треонин
-триптофан
-валин
-аланин
-аргинин
-аспарагин
-аспарагиновая кислота
-цистеин
-глутамин
-глицин
-орнитин
-пролин
-серин
-тирозин
-аргинин
-аспарагин
-аспарагиновая кислота
-цистеин
-глутамин
-глицин
-орнитин
-пролин
-серин
-тирозин
яйца, соевый протеин, кунжут, арахис, пармезан, белая рыба, свинина, говядина, тофу


Различают четыре структуры белков:
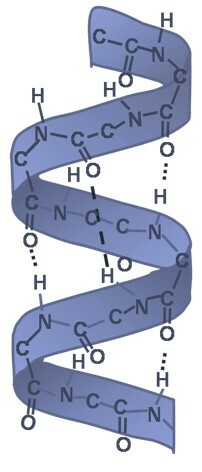
1. Первичная структура – последовательность аминокислот, соединенных пептидными связями.
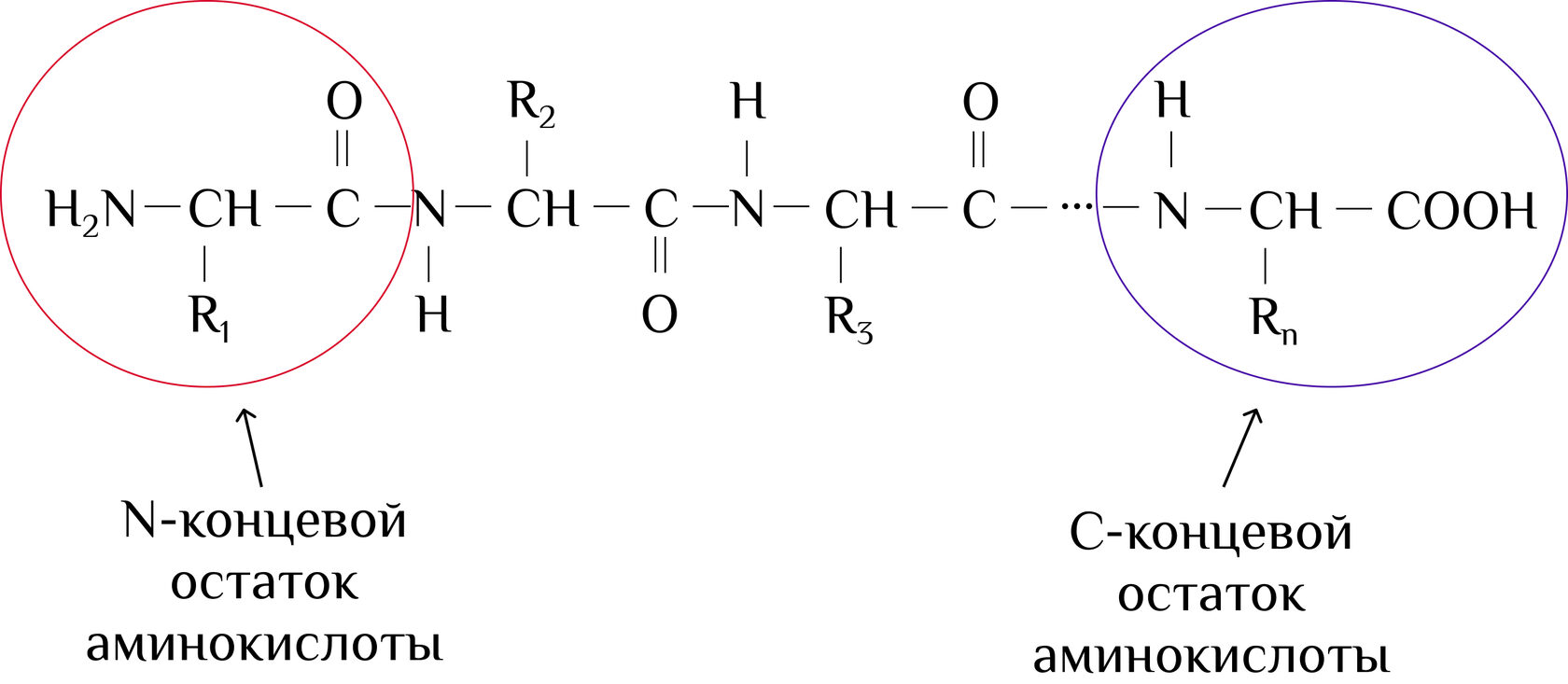
α-спираль
2. Вторичная структура белка – полипептидная цепь, закрученная в α-спираль или β-складчатую структуру.
Она удерживается при помощи водородных связей, которые возникают между NH- и СО-группами, расположенными на соседних витках.
Функционирование в виде закрученной спирали характерно для фибриллярных белков (коллаген, фибриноген, миозин, актин и др.)
Она удерживается при помощи водородных связей, которые возникают между NH- и СО-группами, расположенными на соседних витках.
Функционирование в виде закрученной спирали характерно для фибриллярных белков (коллаген, фибриноген, миозин, актин и др.)
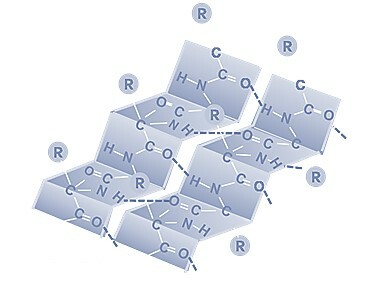



β-структура
Первичная структура (полипептидная цепь)
3. Третичная структура – сворачивание спирали в сложную конфигурацию – глобулу, поддерживаемую:
Многие белковые молекулы становятся функционально активными только после приобретения глобулярной (третичной) структуры.
Многие белковые молекулы становятся функционально активными только после приобретения глобулярной (третичной) структуры.
• дисульфидными связями (–S–S–, возникающими между радикалами серосодержащих аминокислот – цистеина и метионина),
• ионными связями (за счет радикалов)
• гидрофобными взаимодействиями (за счет радикалов)
• ионными связями (за счет радикалов)
• гидрофобными взаимодействиями (за счет радикалов)
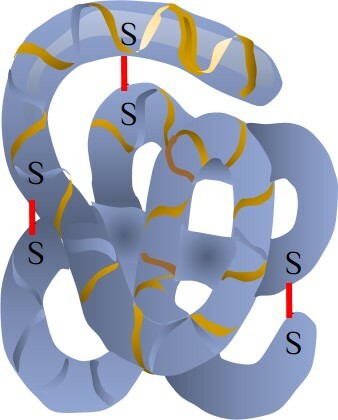

дисульфидная связь
глобула
4. Четвертичная структура белка – взаимное расположение в пространстве нескольких полипептидных клубков, составляющих одну белковую молекулу, образует четвертичную структуру (химические связи могут быть разными).
первичная структура
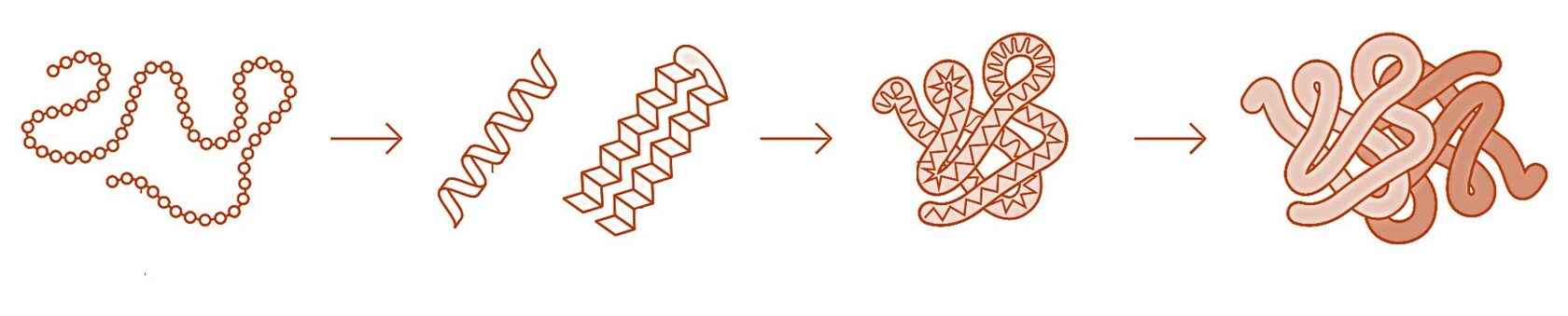
вторичная структура
третичная структура
четвертичная структура
Денатурация и ренатурация
Денатурация – утрата белковой молекулой своей структурной организации, бывает:
-обратимая;
-необратимая.
Ренатурация – восстановление структуры белка.
нативная структура белка
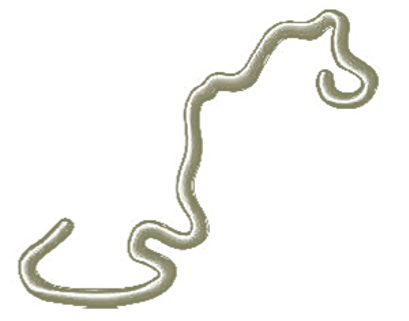

денатурация белка
ренатурация белка



Функции белков
1. Ферментативная (каталитическая): ферменты способны ускорять химические реакции.
Например:
- фермент крови каталаза ускоряет реакцию разложения перекиси водорода на воду и кислород;
- фермент желудочного сока пепсин ускоряет створаживание молока.
обработка раны перекисью водорода


створаживание молока
2. Структурная (строительная): белки являются обязательным компонентом всех клеточных структур, органов и тканей.
Например:
- белок волос – кератин;
- белок хрящевой ткани – коллаген.
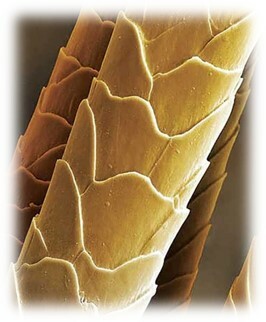
волос под микроскопом
хрящ коленного сустава
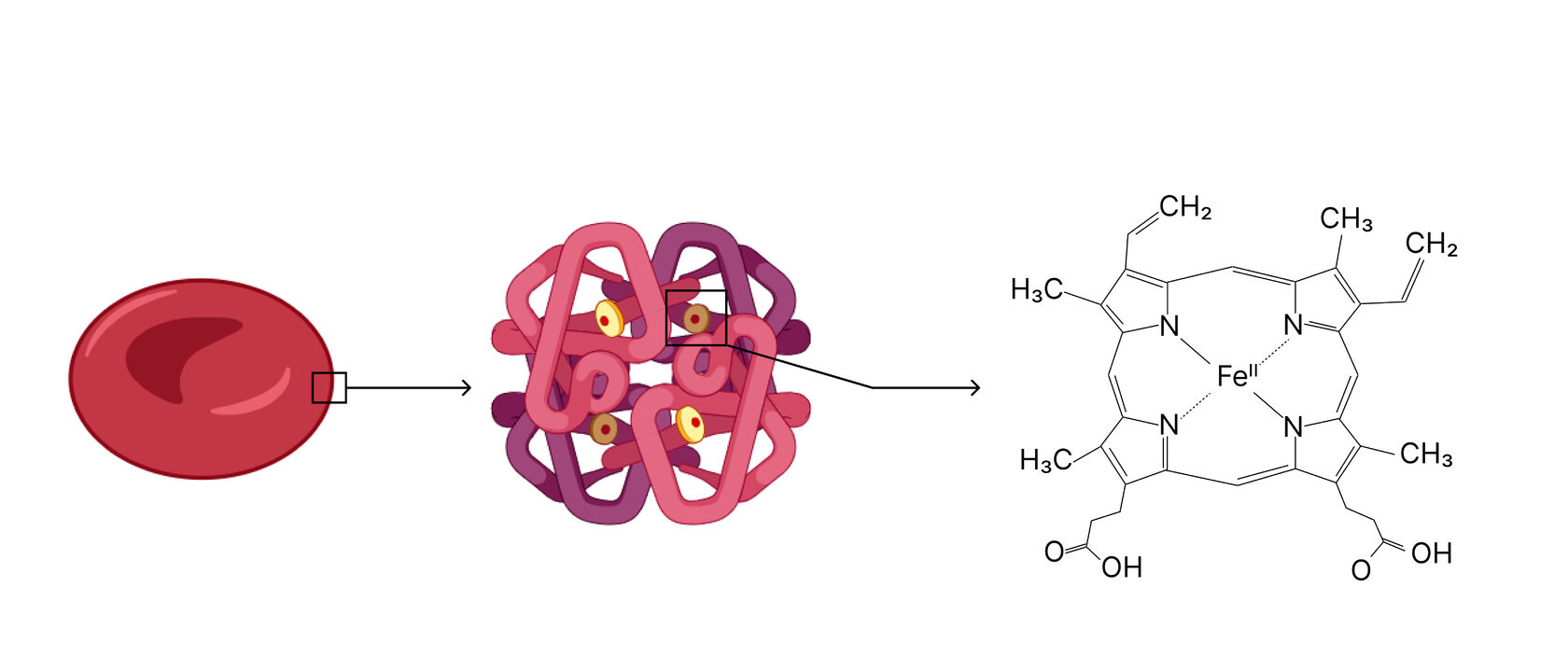
Эритроцит состоит из мембраны, заполненной гемоглобином
3. Транспортная: белки могут быть переносчиками различных веществ.
Например:
Например:
- белок клеток крови — гемоглобин переносит О2;
- белок плазмы крови — трансферрин переносит ионы железа (Fe3+).
4. Двигательная (сократительная): обеспечивают двигательные реакции организмов.
Например:
- сократительные белки мышц – актин и миозин;
- белок жгутиков бактерий – флагеллин.
бактерия
актин
В составе гемоглобина есть белок глобин и гем
Гем – это сложная молекула с атомом железа в центре
Змея выбрасывает яд из ядовитых желез
5. Защитная: выполняют защиту от патогенов, хищников и других опасных факторов.
Например:
Например:
- при попадании инородных тел в организме вырабатываются защитные белки – антитела;
- яд змей, грибов, насекомых – нейротоксины, протеазы и др.
6. Энергетическая: при недостатке углеводов и жиров могут окисляться и молекулы аминокислот.
Энергетическая ценность 1 г белка – 17,6 кДж (~4 ккал) энергии.

Яйцо – источник питательных веществ для зародыша

7. Регуляторная (гормональная): белки регулируют работу внутренних органов.
Например:
Например:
- гормон поджелудочной железы – инсулин, регулирует уровень глюкозы в крови;
- гормон гипофиза – соматотропин, регулирует процессы роста .
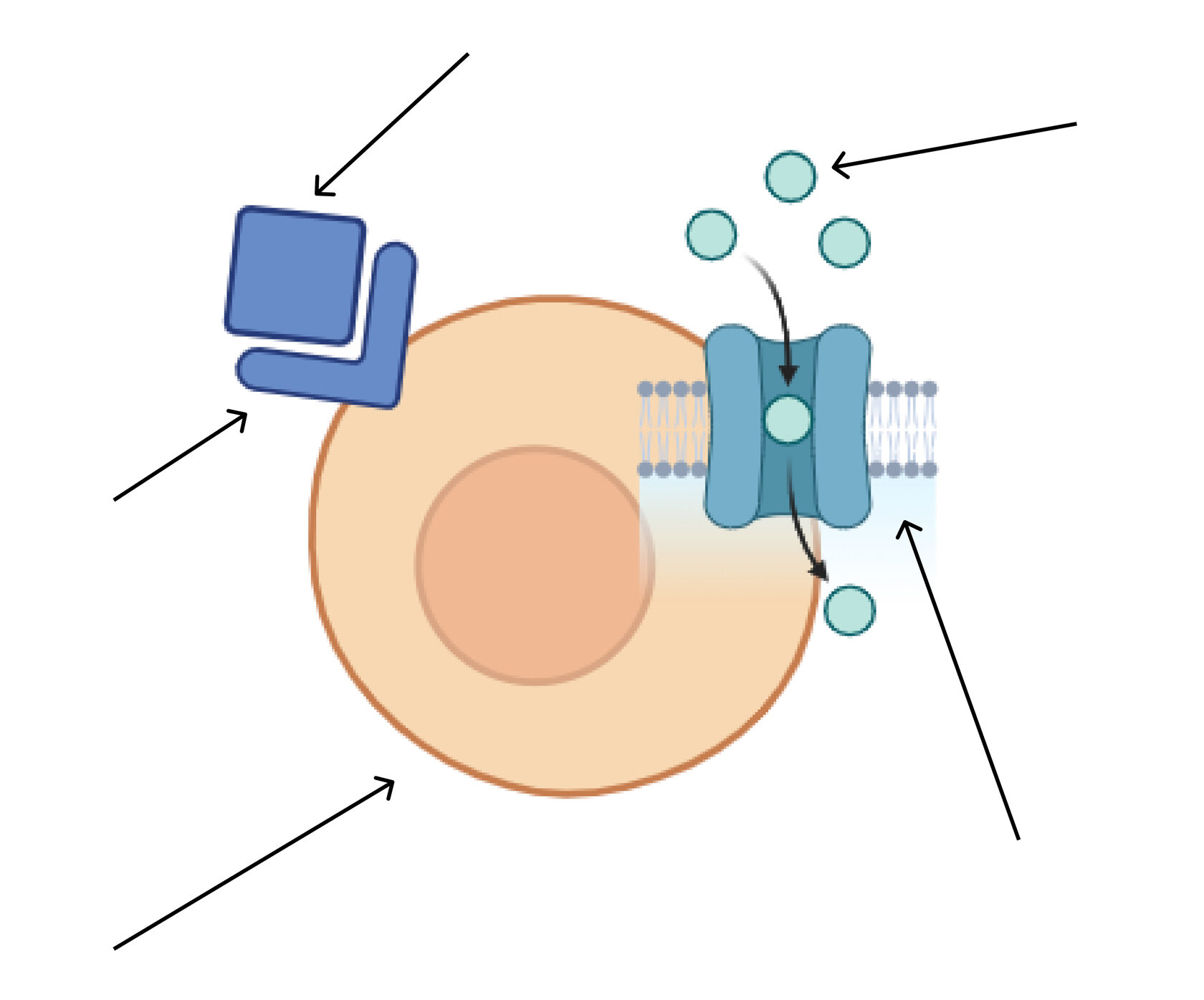
8. Сигнальная (рецепторная): в мембрану встроены особые белки (интегрины), способные изменять свою третичную структуру на действие факторов внешней среды. Так происходит приём сигналов из внешней среды и передача информации в клетку.
цитоплазма
инсулин
Инсулин взаимодействует со своим рецептором на поверхности клетки.
После этого открывается глюкозный канал, проходящий через клеточную мембрану.
По каналу глюкоза поступает в клетку.
После этого открывается глюкозный канал, проходящий через клеточную мембрану.
По каналу глюкоза поступает в клетку.
рецептор инсулина
клетка
глюкоза
глюкозный канал
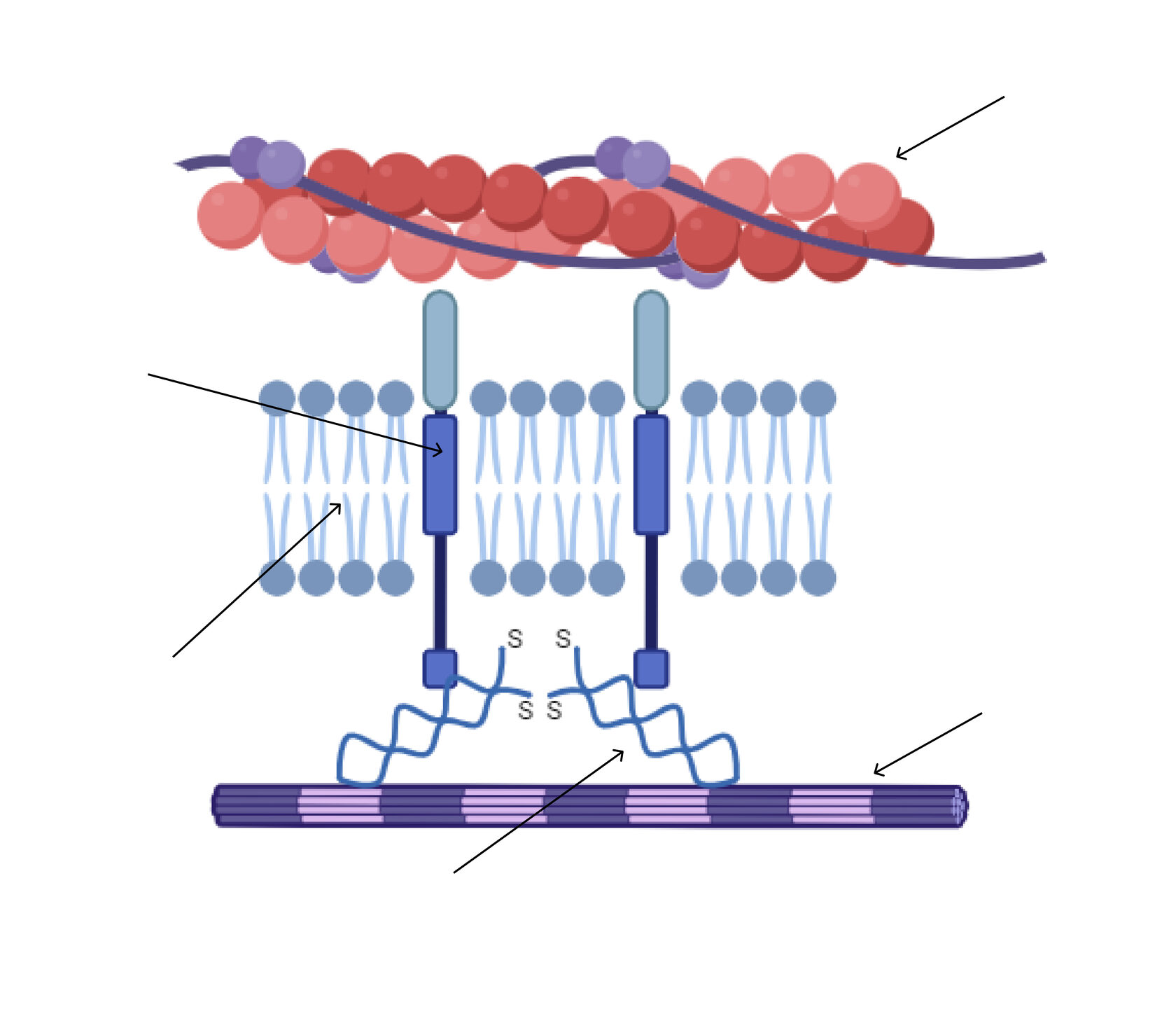
актин
клеточная мембрана
интегрин
коллаген
фибронектин

9. Запасающая: некоторые организмы запасают белки (это нетипичная функция).
Например:
Например:
- в запасающей ткани семени (эндосперме) злаков – глютен;
- запасной белок яичного белка – альбумин.
Семена злаков – источник питательных веществ
Ссылки на материалы для "Уровней организации жизни", взяты с сайта flaticon.com:
1) <a href="https://www.flaticon.com/ru/free-icons/" title="олень иконки">Олень иконки от smashingstocks - Flaticon</a>
Иллюстрации сделаны при использовании biorender.com.
1) <a href="https://www.flaticon.com/ru/free-icons/" title="олень иконки">Олень иконки от smashingstocks - Flaticon</a>
Иллюстрации сделаны при использовании biorender.com.
